Epidemija debljine predstavlja svjetski zdravstveni problem koji ima svoje značajne ekonomske i socijalne posljedice. Procjenjuje se da danas ima oko pola milijarde debelih osoba u svijetu (engl. body mass index – BMI > 30) te preko milijarde njih s prekomjernom težinom (BMI 25 – 30). Najčešće posljedice debljine su metabolički poremećaji poput rezistencije na inzulin perifernih tkiva koja često progredira u šećernu bolest tipa 2 sa brojnim komplikacijama.
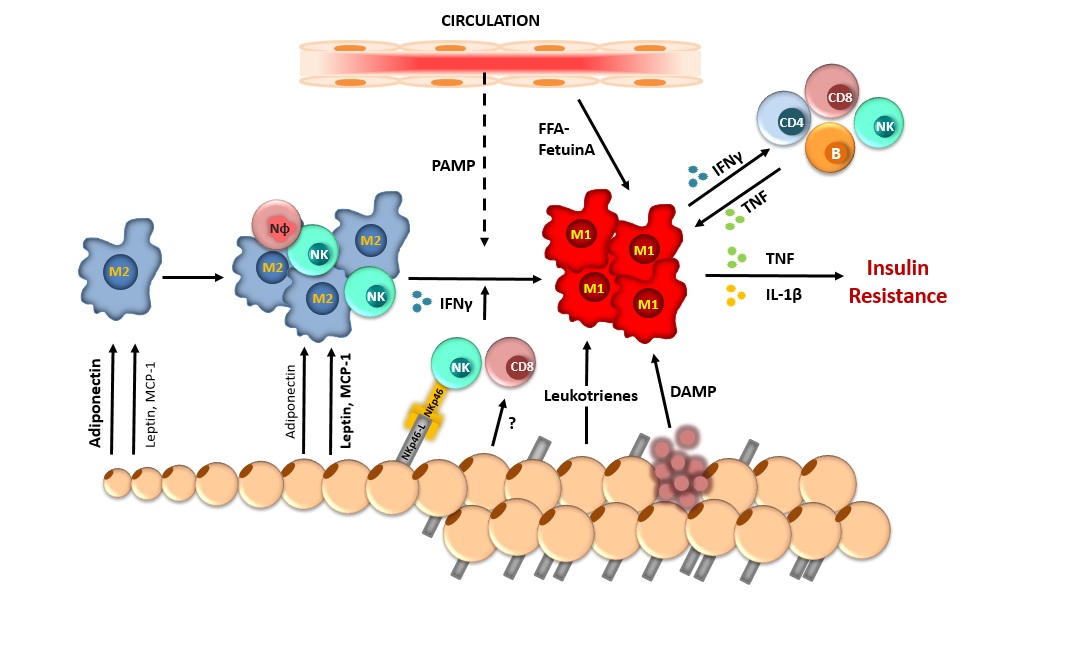 Slika1. Razvoj upale visceralnog masnog tkiva. (Izvor: Wensveen FM, Valentić S., Šestan M., Turk Wensveen T., Polić B. (2015) The “Big Bang” in obese fat: Events initiating obesity‐induced adipose tissue inflammation. Eur J Immunol 45 (9), 2446-2456)
Slika1. Razvoj upale visceralnog masnog tkiva. (Izvor: Wensveen FM, Valentić S., Šestan M., Turk Wensveen T., Polić B. (2015) The “Big Bang” in obese fat: Events initiating obesity‐induced adipose tissue inflammation. Eur J Immunol 45 (9), 2446-2456)
Danas postoji opći konsenzus da je aktivacija imunološkog sustava u visceralnom masnom tkivu (VMT) u debljini izvor razvoja sistemske kronične upale niskog intenziteta. Ona pak predstavlja glavnu podlogu za razvoj rezistencije na inzulin. Istraživanja provedena u posljednjih nekoliko godina, uglavnom na animalnim modelima, pokazuju da dominantnu populaciju stanica čine makrofazi. U mršavih ljudi ili miševa hranjenih normokaloričnom dijetom (5-6 % masti, engl. NCD) ove stanice imaju fenotip protuupalnih M2 makrofaga koji izlučuju Th2 citokine poput IL-4 i IL13 te u interakciji sa drugim stanicama (eozinofili, mastociti, NKT stanice, Treg stanice, ILC2 limfociti) sprječavaju diferencijaciju i privlačenje proupalnih stanica iz cirkulacije. No, u slučaju upotrebe visokokalorične masne hrane (50 – 60% masti, engl. HFD) dolazi do pretvorbe M2 u M1 makrofage koji izlučuju proupalne citokine poput TNFa, IL-1b, IL-6 i dr. To ima značajne učinke na diferencijaciju i proliferaciju proupalnih stanica u samom visceralnom masnom tkivu, ali i na privlačenje drugih proupalnih stanica iz cirkulacije u masno tkivo. Proupalni citokin djeluju sistemski poticanjem upalnog signaliranja i ometanjem signaliranja putem inzulinskog receptora.
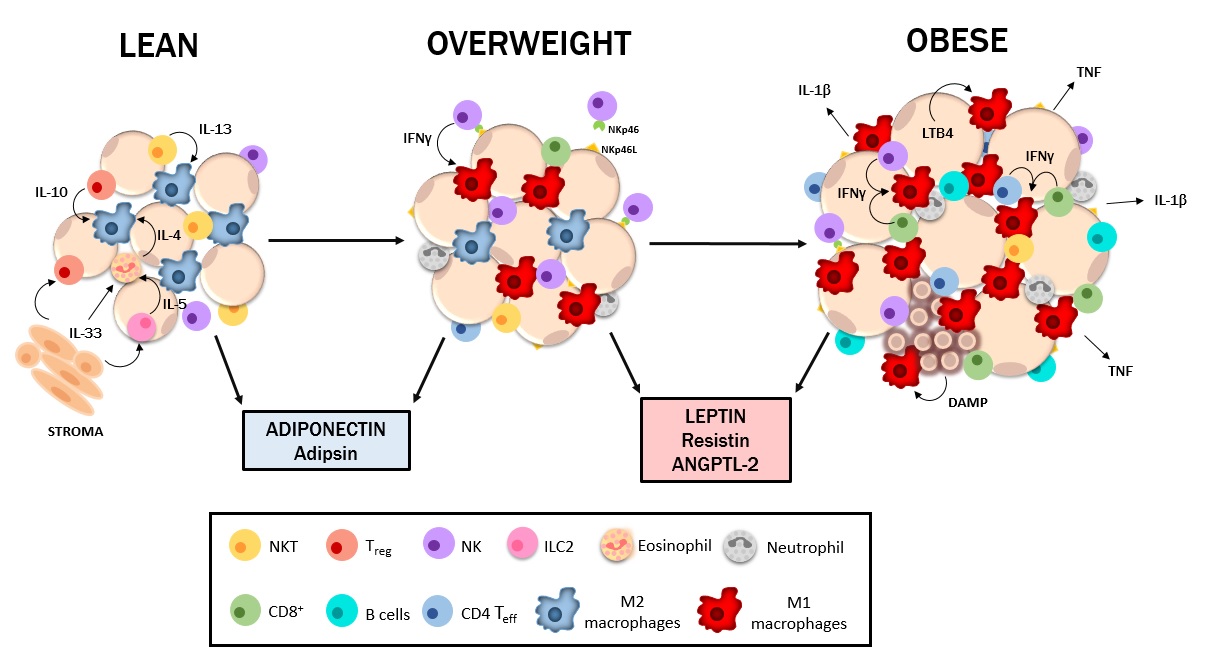 Slika 2. Stadiji upale visceralnog masnog tkiva kao odgovor na upotrebu visokokalorične masne hrane. (Izvor: Wensveen FM, Valentić S., Šestan M., Turk Wensveen T., Polić B. (2015) Interactions between adipose tissue and the immune system in health and malnutrition. Semin Immunol 27 , pp. 322-333)
Slika 2. Stadiji upale visceralnog masnog tkiva kao odgovor na upotrebu visokokalorične masne hrane. (Izvor: Wensveen FM, Valentić S., Šestan M., Turk Wensveen T., Polić B. (2015) Interactions between adipose tissue and the immune system in health and malnutrition. Semin Immunol 27 , pp. 322-333)
Unatoč brojnim studijama koje su učinjene u ovom području, još uvijek nisu posve jasni mehanizni inicijalne aktivacije imunološkog sustava, niti je poznato koje sve stanice imunološkog sustava sudjeluju u tom procesu. Naša je hipoteza da neke od stanica i receptora prirođene imunosti (ILC1, ILC3, gd limfociti T i B1 limfociti, NKG2D, NCR1, gdTCR), koje su prisutne u VMT, imaju važnu ulogu u translaciji metaboličkog stresa adipocita masnog tkiva u upalnu reakciju.
Ova hipoteza je utemeljena na sljedećim preliminarnim rezultatima naših istraživanja: a) visceralno masno tkivo miševa na normalnoj dijeti ima osobit sastav imunoloških stanica u kojem dominiraju makrofagi, ILC stanice, gd limforiti T, a manje su prisutni limfociti adaptive imunosti b) vrlo rano nakon tretmana s HFD dolazi do porasta broja ILC1 i makrofaga, a značajno se povećava i izlučivanje interferona gama (IFNg); c) makrofazi u VMT proliferiraju i konvertiraju se u proupalne M1 makrofage već vrlo rano od početka HFD; d) deplecija IFNg dovodi do prevencije konverzije makrofaga; e) eksperiment na miševima sa teškom kombiniranom imunodeficijencijom (SCID) i bez adaptivne imunosti pokazuje da su oni sposobni razviti inzulinsku rezistenciju; f) Klrk1 k.o. (NKG2D-deficitni) miševi razvijaju inzulinsku rezistenciju puno prije kontrola; g) udio gd limfocita T je u VMT neobično visok (5-6%); h) uočava se značajna prisutnost ILC1 stanica u VMT.
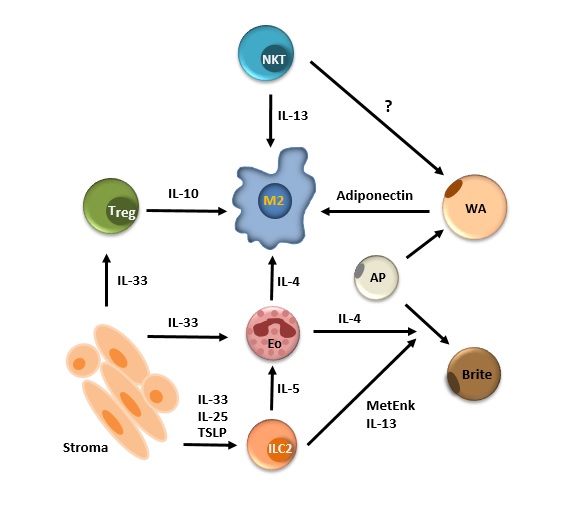 Slika 3. Kontrola homeostaze masnog tkiva u normalnim uvjetima. (Izvor: Wensveen FM, Valentić S., Šestan M., Turk Wensveen T., Polić B. (2015) The “Big Bang” in obese fat: Events initiating obesity‐induced adipose tissue inflammation. Eur J Immunol 45 (9), 2446-2456)
Slika 3. Kontrola homeostaze masnog tkiva u normalnim uvjetima. (Izvor: Wensveen FM, Valentić S., Šestan M., Turk Wensveen T., Polić B. (2015) The “Big Bang” in obese fat: Events initiating obesity‐induced adipose tissue inflammation. Eur J Immunol 45 (9), 2446-2456)
Glavni cilj naših istraživanja u ovom projektu jest istražiti ulogu pojedinih stanica i receptora prirođene imunosti („stanica senzora“) kao što su ILC1, ILC3, gd limfociti T i B1 limfociti te NKG2D, NCR1, gdTCR receptora u translaciji metaboličkog stresa masnih stanica u VMT u aktivaciju imunološkog sustava i razvoj upale.
Specifični ciljevi istraživanja bili bi: a) istražiti koje se stanice prirođene imunosti aktiviraju u VMT unutar prva dva tjedna od tretmana HFD, utvrditi dinamiku aktivacije i citokine koje izlučuju; b) istražiti mehanizme aktivacije ILC1 i njihovu ulogu u procesu razvoja upale; b) istražiti zašto hiperaktivne NK stanice u Klrk1 k.o. miševima dovode do bržeg razvoja inzulinske rezistencije i na koji način; c) istražiti ulogu gd limfocita T, mehanizme njihove aktivacije; d) istražiti ulogu pojedinih subpopulacija prirođenih limfocita (ILC), posebno ILC1 i ILC3 u razvoju procesa upale u VMT; e) istražiti koje su molekule važne za aktivaciju imunološkog sustava izražene u hipertrofičnih adipocita VMT.